5) Molécules polaires
Une molécule est apolaire si elle ne possède pas de liaisons polarisées. Lorsqu’elle possède des liaisons polarisées, une molécule peut être polaire ou apolaire : il faut prendre en compte sa géométrie.
On peut distinguer plusieurs situations :
A) Une molécule diatomique
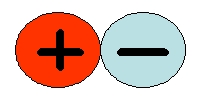
Lorsque la liaison n’est pas polarisée, une molécule diatomique est apolaire.
Une molécule diatomique est polaire lorsque sa liaison est polarisée.
Cas de la molécule de chlorure d'hydrogène :
 |
||
| Charges partielles | Dipôle équivalent |
B) Molécules polyatomiques possédant plus de deux atomes
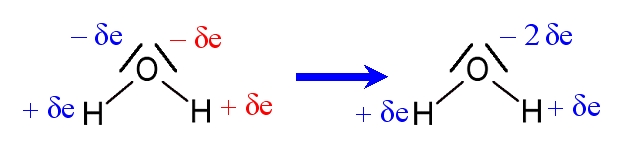
Cas de la molécule d’eau :
Les deux liaisons sont polarisées : chaque liaison peut être assimilée à un dipôle avec une charge partielle positive ( ) sur chaque atome d'hydrogène (élément le plus électropositif) et deux charges partielles négatives ( ) sur l'atome d'oxygène (élément le plus électronégatif).
 |
| Écriture des charges partielles |
La molécule d'eau est coudée : l'angle entre les deux liaisons O-H est voisin de 105°.
Le point représentatif des charges partielles négatives (barycentre) est situé sur l'atome d'oxygène : le pôle "négatif" est situé sur l'atome d'oxygène. Le point représentatif des charges partielles positives est situé entre les deux atomes d'hydrogène : le pôle "positif" est situé entre les deux atomes d'hydrogène.
Les deux points représentatifs sont-ils confondus, placés au même endroit ?
Dans le cas de la molécule d'eau, du fait de sa géométrie coudée, le pôle "positif" n'est pas confondu avec le pôle "négatif". On peut considérer que la molécule présente deux pôles distincts : l'un "négatif", le deuxième "positif" . On dit que la molécule est polaire.
L’eau constituée de molécules polaires est un solvant polaire.
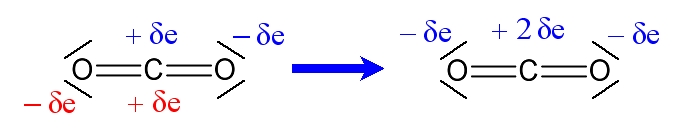
Cas du dioxyde de carbone :
L’oxygène est plus électronégatif que le carbone. Les deux liaisons covalentes C = O d’une molécule de dioxyde de carbone sont donc polarisées. Il en résulte l’apparition de charges partielles ( ) sur chaque atome d’oxygène et d’une charge partielle ( ) sur l’atome de carbone.
Mais la molécule de dioxyde de carbone est une molécule linéaire.
Dans le cas de la molécule de dioxyde de carbone, du fait de sa géométrie linéaire, le pôle "positif" est confondu avec le pôle "négatif". On peut donc considérer que la molécule ne présente pas de dipôles. On dit alors que la molécule est apolaire.
 |
| Écriture des charges partielles |